BEPC PC 2000
BEPC 2000
CHIMIE (Les deux exercices sont obligatoires)
EXERCICE I (SUR 10 POINTS)
1 – On réalise la combustion vive de fer. On obtient un produit grisâtre pouvant être attiré par un aimant dont la masse est égale à 4,64g.
a) Faites le schéma annoté de cette expérience (2pts)
b) Donnez le nom et la formule du produit formé (1pt)
c) Écrivez l’équation bilan de cette réaction chimique (1pt)
d) Calculez : - la quantité (en mol) du produit obtenu (1pt)
- la masse du fer qui a réagi. (1pt)
- le volume du dioxygène qui a réagi, mesuré dans les conditions normales de température et la pression (1pt)
2 – Un clou en fer, neuf est abandonné à l’air humide
a) Que constate-t-on après quelques jours ? (0,5pt)
b) Quel est le nom donné à la réaction chimique qui s’est produite ? (0,5pt)
c) Donner le nom et la formule du réactif gazeux qui a participé à la réaction. (1pt)
d) En admettant que le produit obtenu est composé essentiellement d’oxyde de fer III (Fe2 O3) écrivez l’équation bilan de la formation de ce produit. (1pt)
On donne : M (Fe) = 56g/mol ; M(O) = 16g / mol
EXERCICE 2 (SUR 10 POINTS)
1 – On dissout m = 4g de cristaux d’hydroxyde de sodium dans de l’eau pure. On obtient V = 250cm3 de solution aqueuse. On y ajoute quelques gouttes de BBT
a) Quelle est la teinte prise par la solution ? (1pt)
b) Écrivez l’équation bilan de cette dissolution (1pt)
c) Calculez, en mole la quantité de soluté utilisée (1pt)
d) En déduire les quantités en mole d’ions hydroxyde et d’ions sodium dans la solution. (1pt)
e) Calculez les concentrations massique de la solution (1pt)
f) Calculez les concentrations en ions hydroxyde et en ions sodiums de la solution (1pt)
2 – Un tube à essais contient une solution de chlorure de fer II (ou chlorurez ferreux). La solution a une teinte vert pâle.
a) Quel est l’ion responsable de la teinte prise par l solution ? (1pt)
b) On introduit dans cette solution quelques de solution concentrée d’hydroxyde de sodium. Faites le schéma de l’expérience (2pts)
c) Écrivez l’équation bilan simplifié de la réaction qui se produit. (1pt)
On donne : M(Na) = 23g/mol ; M(O) = 16g/mol ; M(H) = 1g/mol
PHYSIQUE (Les trois exercices sont obligatoires)
EXERCICE D’OPTIQUE (SUR 6POINTS)
1 – La décomposition de la lumière blanche donne diverses sortes de radiations.
a) Quels sont les deux radiations lumineuses extrêmes visibles par l’œil humain ? (1pt)
b) Quels sont les deux types de radiations lumineuses invisibles par l’œil humain ? (1pt)
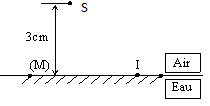
2 – Une radiation lumineuse visible, partant d’une source ponctuelle S, vient frapper au point I un miroir M, placé au dessous de la surface libre d’une eau. (Voir schéma)
a) Quel est le phénomène physique qui se produit ? (1pt)
b) Reproduisez le schéma et tracer le rayon incident (1pt)
c) Construisez géométriquement le rayon réfléchi correspondant (1pt)
3 – On enlève le miroir M. la radiation lumineuse frappe maintenant la surface libre de l’eau et y pénètre. Quel phénomène physique se produit – il alors ? (1pt)
EXERCICE DE MÉCANIQUE (SUR 16 POINTS)
1 – Un corps A de forme parallélépipède, de masse M = 240g et de volume V =400cm3 tombe d’une hauteur h = 5m.
a) Calculez le poids de ce corps. (1pt)
b) Calculez le travail de ce poids. Quelle est la nature de ce travail ? (1,5 pt)
c) Calculez la masse volumique du corps A. (1 pt)
2 – On plonge le corps A dans l’eau.
a) Le corps A va – t – il flotter ou couler ? Justifier votre réponse. (1pt)
b) Quelles sont les forces qui s’exercent sur ce corps ? (1pt)
c) Donnez les caractéristiques de chacune de ces forces. (4pt)
d) Représentez les vecteurs – forces correspondants. (2,5pt)
Échelle : 1 cm pour 0,8N
e) Calculez le volume Vi de la partie immergée du corps A. (1pt)
3- On pose un corps B de masse m sur le corps A. Le corps A est alors complètement immergé dans l’eau. Le système composé des corps A et B est en équilibre. (Voir schéma ci – dessous).
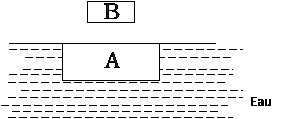
a) Calculer l’intensité de la poussée d’Archimède qui s’exerce sur le système. (1pt)
b) Calculez le poids du corps B. (1pt)
c) En déduire sa masse. (1pt)
On donne : g = 10N/kg
Masse volumique de l’eau : a = 1g/cm3
EXERCICE D’ÉLECTRICITÉ (Sur 18 points)
Voici le schéma d’une installation électrique à la maison. Ce schéma comporte des erreurs et des outils.
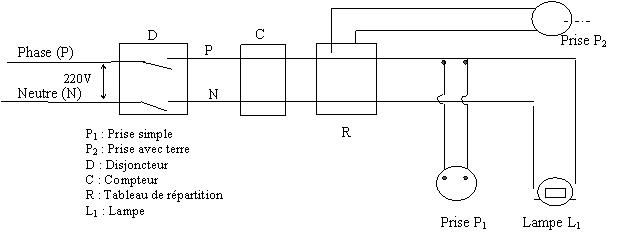
1 – Reproduire sur votre feuille le schéma correct (4pts)
2 – a) Dans le schéma précédent, quel est le rôle : - du disjoncteur D ? (0,5pt)
- Du compteur C ? (0,5pt)
b) A quoi sert un fusible ? Un interrupteur ? (1pt)
3 – Citer deux règles de sécurités pour éviter l’électrocution. (2pts)
4 – La lampe L1 utilisée dans cette installation porte les indications suivantes : (220V, 60W)
Sur la prise P1 est branché un fer à repasser portant les indications suivantes : (220V, 1100W)
a) Que signifient les inscriptions lues sur la lampe L1 ? (1pt)
b) Comment sont branchés la lampe L1 et le fer à repasser ? (0,5pt)
c) Calculez la résistance à chaud du fer à repasser en fonctionnement normal ? (1pt)
d) Calculez la puissance électrique totale, consommée dans cette installation. (1pt)
e) Calculez en joule puis en wattheure, l’énergie totale consommée dans cette installation pendant 1 heure de fonctionnement (1,5pts)
f) Calculez le prix de cette énergie électrique si le kilowattheure vaut 475Fmg. (1pt)
5 – Voici le schéma d’un montage électrique réalisé en classe.
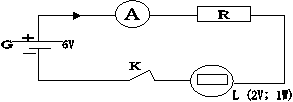
La lampe L s’allume normalement
a) Comment sont branchés la lampe L et le résistor R ? (1pt)
b) Quelle est l’indication de l’ampèremètre A ? (1pt)
c) Déterminez la tension aux bornes du résistor. (1pt)
d) Calculez la résistance R du résistor. (1pt)

