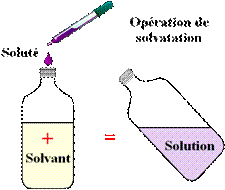
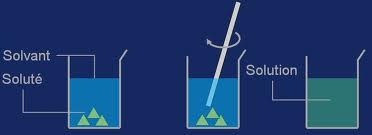
Solvant soluté solution
Rappels : Solvant, soluté, solution et concentration massique
1- Solvant- Soluté – Solution
1-1 Définitions
Le solvant est un liquide qui dissout
Le soluté est un corps qu’on dissout dans le solvant
La solution est un mélange homogène obtenu d’un solvant et d’un soluté
1-2 Remarque
Lorsque le solvant est l’eau donc la solution est dite aqueuse
1-3 Exemple : le thé sucré
Le solvant : eau
Le soluté : thé en poudre, sucre
La solution : thé sucré
NaCl ![]() Na+
+ Cl- : solution aqueuse de chlorure de sodium
Na+
+ Cl- : solution aqueuse de chlorure de sodium
NaOH
![]() Na+ + OH- :
solution aqueuse d’hydroxyde de sodium (soude)
Na+ + OH- :
solution aqueuse d’hydroxyde de sodium (soude)
HCl ![]() H+
+ Cl- : solution aqueuse d’acide chlorhydrique
H+
+ Cl- : solution aqueuse d’acide chlorhydrique
H2SO4
![]() 2H+ +SO42- :
solution aqueuse d’acide sulfurique
2H+ +SO42- :
solution aqueuse d’acide sulfurique
2- Concentrations massique et molaire
2-1 La concentration massique
La concentration massique Cma est la masse de soluté dissout dans un litre de solution donnée par la formule
![]()
2-2 La concentration molaire d’une solution
La concentration molaire d’une solution notée Cmo ou [A] est le nombre mole (la quantité) de soluté dissout dans un litre de solution donnée par la formule.
|
2-3 Relation entre la concentration molaire et concentration massique
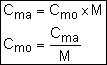
Avec
n : nombre de mole de soluté
V : volume de la solution
M : masse molaire de soluté
m : masse de soluté
2-4 Exemple
On donne 8g de NaOH dans 250cm3.
- La concentration massique :
![]()
![]()
![]()
- La concentration molaire :
![]()
![]()
![]()
![]()